Горючие свойства газа
Основные теплофизические и горючие свойства газа простых горючих и балластных газов, входящих в состав различных видов газового топлива, приедены в табл. 1-4, 1-5, 1-6.
Таблица 1-4. Теплофизические свойства углеводородов метанового ряда (алканов).
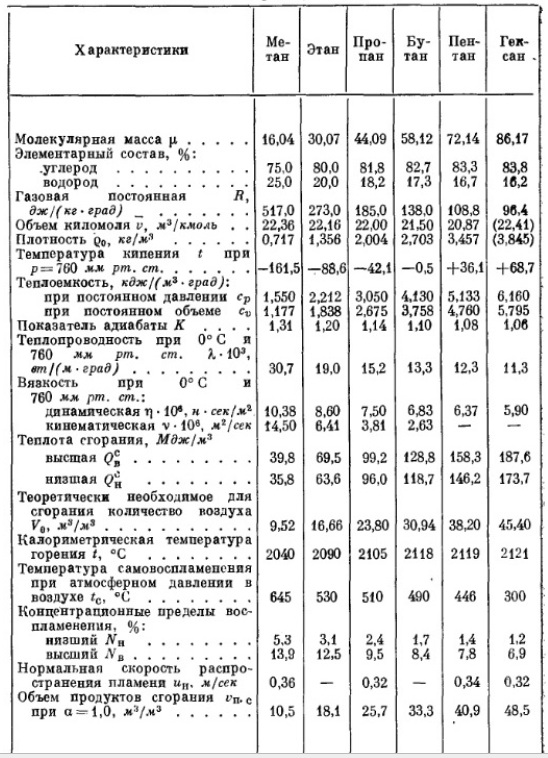
Таблица 1-5. Теплофизические свойства некоторых горючих газов.
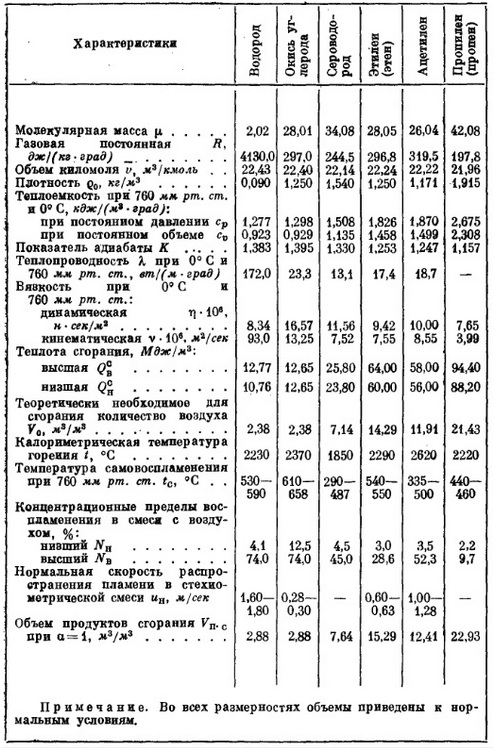
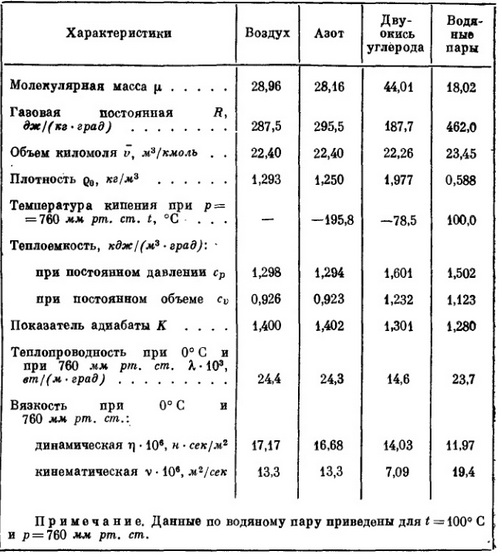
Таблица 1-6. Физико-химические свойства балластных газов и воздуха.
Основные понятия и определения.
1. Молекулярная масса - это сумма атомных масс элементов, входящих в состав молекулы.
2. Элементарный состав газа - массовые доли элементов, приходящиеся на 1 кг газа и выраженные в процентах. Массовая доля элемента может быть подсчитана по формуле
gk=µkn/µ*100 [100%], (I-1)
где gk - доля элемента k, %;
µk - атомная масса элемента к;
n - число атомов элемента к в молекуле газа;
µ - молекулярная масса газа.
3. Газовая постоянная R, кдж/(кг*град) - работа 1 кг газа в изобарном процессе при нагревании его на 1° С. Газовая постоянная в уравнении состояния связывает основные параметры газа.
4. Объем киломоля v, м3/кмоль - объем, занимаемый µ кг газа. Объем киломоля идеального газа является постоянной величиной, равной в нормальных условиях 22,4 м3. Для реальных газов объем киломоля несколько отличается от приведенной величины.
5. Плотность q, кг/м3 - масса газа в объеме 1 м3. В справочных таблицах теплофизических характеристик как объем киломоля, так и плотность газа приводятся для нормальных условий, т. е. для давления в 101 300 н/м2 (760мм. рт. ст.) и температуры 273,15° К (0°С).
6. Температура кипения - температура, при которой упругость паров над поверхностью жидкости равна внешнему давлению, т. е. температура равновесия между жидкой и паровой фазами при давлении р.
7. Теплоемкость удельная - количество тепла, необходимой для нагревания единицы количества тела (газа) на 1° С. Для газов за единицу количества принимают массу в 1 кг (массовая теплоемкость) или 1 м3 в нормальных условиях, т. е. q0, кг. Как известно, величина теплоемкости газа зависит от термодинамического процесса, при котором происходит сообщение тепла. В термодинамических соотношениях и расчетах различают две теплоемкости: теплоемкость в процессе нагревания газа при постоянном давлении - ср и то же, при постоянном объеме - сv.
8. Показатель адиабаты К - отношение теплоемкостей cp/cv
9. Коэффициент теплопроводности λ, вт/(м*град) - количество тепла, передаваемого в единицу времени через 1 м2 поверхности, нормальной к направлению потока (т. е. мощность теплового потока) при градиенте температуры 1 град/м.
Коэффициент теплопроводности определяет только молекулярный перенос энергии. Величина Я значительно увеличивается с повышением температуры газа и незначительно зависит от давления.
10. Коэффициент вязкости (динамической) η, н* сек/м2 - коэффициент внутреннего трения газа или жидкости, обусловленный внутримолекулярным состоянием, благодаря которому в газе или жидкости, движущихся с деформацией элементарных объемов, возникают силы трения.
В технических расчетах обычно имеют дело с коэффициентом кинематической вязкости v, представляющим собой отношение коэффициента динамической вязкости к плотности, т. е.
v =η/q [м2/сек], (I-2)
С повышением температуры вязкость газов увеличивается.
Весьма важными характеристиками газов являются их горючие свойства газа. Понятно, что в данном случае речь идет только о горючих газах.
Горение в техническом понимании представляет собой процесс окисления горючих компонентов топлива кислородом воздуха, сопровождающийся выделением тепла. Этот процесс может протекать при определенном уровне энергии молекул горючего и окислителя.
1. Теплота сгорания Qc, дж/м3 - количество тепла, выделяющегося при полном сгорании единицы количества топлива. Единицей количества для газового топлива обычно считают 1 м3 при нормальных условиях, т. е. q0, кг газа.
Различают высшую (Qсв) и низшую (Qсн) теплоты сгорания. Высшая теплота сгорания определяется количеством тепла, выделяющегося при сгорании единицы количества топлива, включая теплоту водяных паров, содержащихся в продуктах сгорания.
За основную расчетную величину обычно принимают низшую теплоту сгорания, т. е. теплоту сгорания топлива без учета теплоты водяных паров при давлении 760 мм. рт. ст. и 0° С.
2. Теоретическое количество воздуха, необходимое для сгорания 1 м3 газа V0, м3/м3 - величина, определяемая из стехиометрического уравнения реакции горения и содержания кислорода в атмосферном воздухе.
3. Калориметрическая температура горения t, °С - температура, которую могли бы иметь продукты сгорания при полном сгорании газа с учетом всего тепла, вносимого в топку с действительным количеством воздуха. В табл. 1-4 и 1-5 приведены калориметрические температуры при tвоз = tгаз = 0° С и α = 1.
Калориметрическая температура при этих условиях многими авторами называется жаропроизводительностью (термин Д. И. Менделеева).
В отличие от калориметрической теоретическая температура горения определяется с учетом явления диссоциации С02 и Н20.
4. Температура самовоспламенения tc, °С - температура газо-воздушной или газокислородной смеси, при которой начинается интенсивный саморазогрев этой смеси за счет цепного развития реакции окисления.
Температура самовоспламенения не является константой, а зависит от состава смеси, наличия в газе примесей, давления и особенностей ограждающих стенок.
5. Концентрационные пределы воспламенения, % - минимальный (низший предел NH) и максимальный (высший предел NB) - пределы содержания горючие свойства газа в смеси с воздухом или кислородом, когда при зажигании от постороннего источника возможен процесс горения. Концентрационные пределы воспламенения зависят от температуры смеси, наличия балластных примесей и давления.
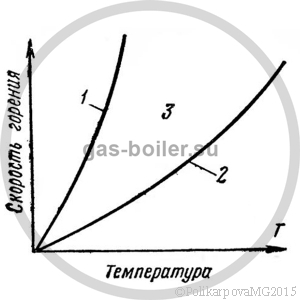
6. Нормальная скорость распространения пламени uн, м/сек - скорость перемещения фронта пламени по нормали к элементу поверхности этого фронта (без образования ударной детонационной волны). Нормальная скорость распространения пламени зависит от природы газа, состава смеси, ее температуры и давления.
7. Объем продуктов сгорания Vп.с, м3/м3 - стехиометрическая характеристика любого горючего, легко определяемая из уравнения полного горения при теоретически необходимом количестве воздуха.
Горючие свойства газа, характеристики простых газов, как температура самовоспламенения, концентрационные пределы воспламенения, нормальная скорость горения, для многих газов исследованы недостаточно полно.