Химические свойства газа
Любое газовое топливо представляет собой смесь различных простых горючих и балластных газов. Химические свойства газа определяют свойства смеси, т. е. газового топлива.
Алканы, т. е. углеводороды предельного ряда, являются основными составляющими горючей части природных и попутных газов. Алканы нередко называют парафинами или углеводородами метанового ряда. Общая химическая формула алканов - СnН2n+2. Родоначальником ряда алканов является метан - СН4, далее, по мере увеличения числа атомов углерода в молекуле, следуют: этан - С2Н6, пропан - С3Н8, бутан - С4Н10, пентан - C5H12, гексан - С6Н14 и т. д.
Физические и химические свойства газа предельных углеводородов закономерно изменяются по мере увеличения их молекулярного веса.
В нормальных условиях, т. е. при температуре 0° С и давлении 760 мм рт. ст., первые члены ряда до бутана включительно - газы, не имеющие цвета и запаха, последующие - жидкости. Все алканы, кроме метана, имеют плотность выше плотности воздуха.
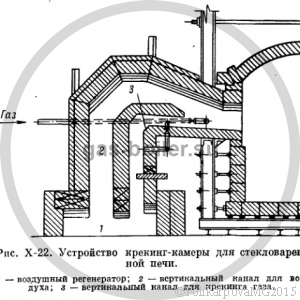
Под действием высокой температуры алканы расщепляются, переходят в более простые и стойкие соединения (например, метан, а также алкены), выделяя сажистый углерод и водород. Стойкость алканов против воздействия температуры снижается с увеличением молекулярной массы.
Содержание углеводородов тяжелее бутана - пентана даже в "сыром" природном газе (т. е. не подвергавшемся обработке) незначительно, поэтому при расчетах химические свойства газа ограничиваются пентаном, суммируя с ним все последующие углеводороды.
Алканы, как и продукты их полного сгорания, не являются ядовитыми. Имеются данные, что высокомолекулярные предельные углеводороды при больших концентрациях в воздухе обладают слабым наркотическим действием.
Алкены, или олефины, входят в заметных количествах в состав искусственных газов, особенно газов крекинга жидкого топлива. Родоначальником ряда алкенов является этилен. Общая химическая формула алкенов - СnН2n- Первые три члена этого ряда - этилен (этен) - С2Н4, пропилен (пропен) - С3Н6 и бутилен (бутен) - С4Н8.
Алкены, являющиеся непредельными углеводородами, представляют собой ценное сырье для химической промышленности.
Токсическое действие алкенов сходно с действием алканов, т. е. при высоких концентрациях они обладают наркотическими свойствами.
Водород Н2 имеется во всех искусственных газах. Это горючий газ, не имеющий запаха и цвета, не токсичен. Водород является самым легким из газов, он в 14,5 раз легче воздуха, поэтому низшая объемная теплота его сгорания меньше, чем у других компонентов газового топлива.
Сероводород H2S содержится в большинстве искусственных и некоторых природных газах. Это бесцветный горючий газ тяжелее воздуха (плотность - 1,54 кг/м3), с сильным запахом, напоминающим запах тухлых яиц. Вызывает сильную коррозию металлов.
Сероводород ядовит. Он действует на нервную систему, а также на дыхательные пути и глаза. При концентрациях сероводорода выше 1 мг/л смертельное отравление может произойти почти мгновенно от паралича дыхательных центров. Допустимая концентрация его в воздухе помещений установлена не более 0,01 мг/л, а в газе, поступающем в городские сети, - не болев 2 г на 100 м3. Высокая токсичность сероводорода и строгие требования к его содержанию вызывают необходимость очистки газового топлива перед подачей его потребителям.
Окись углерода СО в большом количестве содержится в генераторных газах, являясь наряду с водородом основным горючим компонентом.
Окись углерода - химически стойкий горючий газ, не имеющий цвета. Плотность СО (1,25 кг/м3) незначительно ниже плотности воздуха.
Окись углерода является сильным ядом; концентрация его в воздухе в 1% приводит через 1-2 мин к сильному отравлению и смерти. Предельная концентрация СО в воздухе рабочей зоны цехов по существующим нормам не более 0,03 мг/л при длительной работе и не более 0,05 мг/л при пребывании в загазованной атмосфере до 1 ч.
Окись углерода является продуктом неполного сгорания углерода и может находиться в продуктах сгорания любого топлива, содержащего углерод или углеродные соединения.
Сероуглерод CS2 в небольших количествах входит в состав газов, получаемых при сухой перегонке топлив, содержащих серу. Температура кипения сероуглерода +46° С, т. е. при обычных условиях он является жидкостью. Пары сероуглерода в 2,6 раза тяжелее воздуха. Высокие концентрации паров сероуглерода в воздухе приводят к отравлению. Предельно допустимая концентрация в рабочей зоне 0,01 мг/л.
Цианистый водород HCN - сильнейший яд, содержащийся в небольших количествах в газах сухой перегонки топлива. Предельное содержание HCN в газах, применяемых для городского газоснабжения, Пе выше 0,05 мг/л, предельно допустимая концентрация в воздухе промышленных предприятий - 0,0003 мг/л.
Кроме перечисленных выше горючих газов и паров искусственные газы содержат некоторое количество смол, аммиака, нафталина. Эти соединения, представляющие большую ценность для химической промышленности, извлекаются из газового топлива в установках улавливания или очистки газа.
В качестве балластных примесей во всех газах, как природных, так и искусственных, имеются азот N2, водяные пары Н2О и двуокись углерода СО2. Азот и двуокись углерода не токсичны и не агрессивны, т. е. не обладают коррозионными свойствами. Наличие водяных паров может привести к образованию конденсата, усиленной коррозии трубопроводов и образованию гидратных пробок при дальнем транспорте природного газа. Во избежание этого природные и попутные газы перед подачей в магистральные трубопроводы подвергают осушке, при которой одновременно удаляется и двуокись углерода.