Процессы при горении газа
Горение газового топлива представляет собой совокупность сложных аэродинамических, тепловых и химических процессов. Первый из них - процесс смесеобразования - предшествует горению, осуществляясь до ввода газа и воздуха в топку или же одновременно с подачей газа и воздуха.
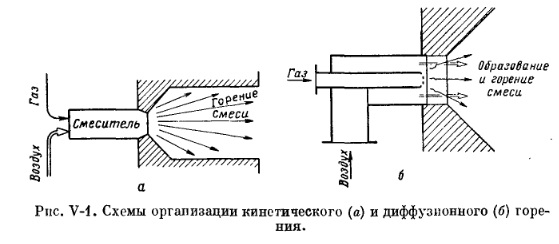
В зависимости от места подготовки горючей газовоздуншой смеси различают кинетическое и диффузионное горение. При кинетическом горении смесь с минимально необходимым или избыточным количеством воздуха приготовляется вне топки, обычно в смесителе горелки. Такое смесеобразование идет без внешнего теплового воздействия на процессы при горении газа. В пределах топки происходят лишь процессы нагрева и воспламенения смеси и стабилизация фронта пламени. При диффузионном горении газ и воздух подводятся к месту сгорания (топке) раздельно, где и образуется горючая смесь.
Процессы при горении газа смесеобразования подчиняются законам молекулярной и турбулентной диффузии. В промышленных установках преобладает последняя. Полная продолжительность процесса диффузионного горения
τ=τд+τгор,
где τд - продолжительность диффузии горючего газа и окислителя, приводящей к созданию однородной смеси;
τгор - продолжительность горения, начиная от разогрева смеси до завершения реакции. Обычно разогрев протекает одновременно со смесеобразованием.
Очевидно, что полная продолжительность процесса при кинетическом горении определяется совокупностью тепловых и химических факторов и подчиняется, с известными ограничениями, законам химической кинетики.
Под кинетикой химической реакции понимают совокупность закономерностей, определяющих ход реакции во времени. Для реакций, протекающих в потоках, течение во времени равнозначно их течению в пространстве. Схемы организации двух видов горения приведены на рис. V-1.
Если происходит предварительное смешение газа с недостаточным количеством воздуха, то полное сгорание возможно лишь, при дополнительном подводе последнего к факелу, т. е. и в этом случае горение будет в известной степени иметь диффузионный характер. Несколько иная картина получается
при предварительном смешении газа с необходимым количеством воздуха, но при незавершенности этого - смешения. В этом случае оно будет заканчиваться в пределах топки, хотя дополнительная подача воздуха и не потребуется. Оба последних вида горения являются промежуточными между кинетическим и диффузионным, но каждый из них обладает своей спецификой, о которой будет сказано ниже.
Реакции окисления горючих элементов топлива могут протекать при низких температурах за счет соударения отдельных немногочисленных молекул, обладающих энергией, превышающей минимальный уровень, достаточный для разрушения внутримолекулярных связей. Однако такое окисление происходит крайне медленно и в обычных условиях не приводит к развитию процесса.
Вторым видом медленного окисления горючих элементов при температурах, не достигающих температуры воспламенения, является горение на поверхности катализатора. Хотя процесс каталитического горения может протекать достаточно интенсивно, он все же не является процессом горения в техническом его понимании и может интересовать теплотехников главным образом с точки зрения применения его для избирательного сжигания газов в целях анализа.
Отличительной чертой технического горения топлива является то, что оно, раз начавшись, способно продолжаться, обеспечивая за счет большого тепловыделения поддержание температуру процесса выше температуры воспламенения, несмотря на непрерывный отвод тепла. Естественно, что такой процесс может протекать при непрерывном поступлении в зону горения и вовлечении в процесс свежего топлива и воздуха.
В § IV-3 нами были рассмотрены некоторые закономерности, относящиеся к кинетике химических реакций, в частности выражения скорости реакции. Рассмотрим дополнительно некоторые вопросы кинетики гомогенного горения.
Следует сразу же заметить, что процессы при горении газа, как это было установлено Н. Н. Семеновым, не подчиняется классическим законам химической кинетики, однако рассмотрение их необходимо для правильного понимания и качественной оценки процессов горения газового топлива.
Вернемся к формуле (IV-1) скорости мономолекулярной реакции. Очевидно, что
dс/С=-kdτ
откуда следует, что при постоянной температуре и k = const
C = C0e-kт, (V-l)
где С0 - начальная концентрация вещества.























